Acido benzoico
| Acido benzoico | |||
|---|---|---|---|
| |||
 | |||
| Nome IUPAC | |||
| acido benzoico | |||
| Nomi alternativi | |||
| acido benzencarbossilico acido benzenmetanoico carbossibenzene | |||
| Caratteristiche generali | |||
| Formula bruta o molecolare | C7H6O2 | ||
| Massa molecolare (u) | 122,13 | ||
| Aspetto | polvere bianca cristallina | ||
| Numero CAS | 65-85-0 | ||
| Numero EINECS | 200-618-2 | ||
| PubChem | 243 | ||
| DrugBank | DB03793 | ||
| SMILES |
C1=CC=C(C=C1)C(=O)O |
||
| Proprietà chimico-fisiche | |||
| Densità (g/cm3, in c.s.) | 1,3 | ||
| Costante di dissociazione acida a 298 K | 6,45×10−5 | ||
| Temperatura di fusione | 120 °C (248F) | ||
| Temperatura di ebollizione | 249 °C (522 K) | ||
| Proprietà termochimiche | |||
| ΔfH0 (kJ·mol−1) | −385,2 | ||
| S0m(J·K−1mol−1) | 167,6 | ||
| C0p,m(J·K−1mol−1) | 146,8 | ||
| Indicazioni di sicurezza | |||
| Punto di fiamma | 121 °C (394 K) | ||
| Temperatura di autoignizione | 570 °C (843 K) | ||
| Simboli di rischio chimico | |||

| |||
| attenzione | |||
| Frasi H | 315 - 318 - 372 | ||
| Consigli P | 280.3 - 302+352 - 305+351+338 - 314 | ||
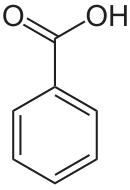
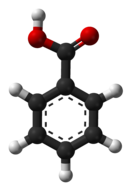
L'acido benzoico (E210) è un acido carbossilico aromatico e ha formula Ph-COOH.
È un solido bianco in forma polverulenta o granulare. L'acido benzoico è leggermente solubile in acqua e solubile in etanolo, molto solubile in benzene ed acetone. La sua soluzione acquosa è debolmente acida.
L'acido benzoico si trova naturalmente in molte piante e funge da intermedio nella biosintesi di metaboliti secondari.
I sali e gli esteri dell'acido benzoico sono noti come benzoati, e sono usati come conservanti alimentari. L'acido benzoico è un importante precursore per la sintesi industriale di molte altre sostanze organiche.
Il nome acido benzoico deriva dalla resina di benzoino che è stata per lungo tempo la sua unica fonte conosciuta, che contiene fino al 20% di acido benzoico e il 40% di esteri dell'acido benzoico.
Indice
Storia
L'acido benzoico fu scoperto nel sedicesimo secolo. La distillazione a secco della gomma di benzoino fu descritta per la prima volta da Nostradamus (1556), e poi da Alessio Piemontese (1560) e Blaise de Vigenère (1596).
Nel 1830 Pierre Robiquet e Antoine Boutron-Charlard, due chimici francesi, grazie a degli esperimenti sull'amigdalina, ottenuta dalle mandorle amare produssero la benzaldeide, ma non riuscirono a dare una corretta interpretazione della struttura dell'amigdalina che contiene il radicale benzoile. Nel 1832 Justus von Liebig e Friedrich Wöhler, determinarono la composizione dell'acido benzoico, studiando anche la sua correlazione con l'acido ippurico. Nel 1875 Salkowski scoprì le capacità antifungine dell'acido benzoico, che fu usato per lungo tempo nella conservazione dei frutti di mirtillo.
Produzione
L'acido benzoico è principalmente prodotto facendo reagire il toluene con ossigeno ad una temperatura di 200 °C e usando sali di cobalto e manganese come catalizzatori; anche altri agenti ossidanti possono essere impiegati, quali il permanganato di potassio, l'acido nitrico o l'anidride cromica.

Essendo molto solubile in acqua calda, e meno solubile in acqua fredda, l'acido benzoico può essere purificato mediante ricristallizzazione dall'acqua, con una resa del 65% circa. L'assenza di solventi organici per la ricristallizzazione rende questo esperimento sicuro.
Il primo processo industriale per la produzione di acido benzoico veniva effettuato sfruttando la reazione del triclorometilbenzene con idrossido di calcio in acqua, usando come catalizzatore il ferro o i suoi sali. Il benzoato di calcio risultante viene convertito in acido benzoico con acido cloridrico. Il prodotto conteneva quantità significative di derivati dell'acido benzoico clorurati. Per questo motivo, l'acido benzoico per il consumo umano venne poi ottenuto per distillazione a secco della gomma benzoina. Oggi l'acido benzoico alimentare è prodotto sinteticamente.
Altri metodi di preparazione sono:
- l'ossidazione dell'alcol benzilico, della benzaldeide o dell'acido cinnamico;
- l'idrolisi del benzonitrile e della benzammide;
- la reazione fra il bromuro di fenilmagnesio (un reattivo di Grignard formato dal bromobenzene) o fenillitio con anidride carbonica;
- la reazione con permanganato di potassio o altri reagenti ossidanti in acqua. La miscela viene filtrata a caldo per rimuovere il biossido di manganese e lasciata raffreddare per formare acido benzoico;
- la reazione del benzil cloruro con KMnO4 alcalino; C6H5CH2Cl + 2 KOH + 2 [O] → C6H5COOH + KCl + H2O
- lareazione dell'acetofenone in ambiente basico con ipoclorito di sodio, ottenendo acido benzoico e cloroformio come sottoprodotto (reazione dell'aloformio).
Reazioni
Le reazioni di acido benzoico possono verificarsi nell'anello aromatico o nel gruppo carbossilico.
La reazione di sostituzione aromatica elettrofila avviene principalmente in posizione 3 a causa del gruppo carbossilico.
Le reazioni degli acidi carbossilici sono possibili anche nell'acido benzoico:
- Gli esteri dell'acido benzoico sono il prodotto della reazione catalizzata da acidi con alcoli.
- Le ammidi dell'acido benzoico sono facilmente disponibili utilizzando derivati dell'acido (come il benzoil cloruro) o accoppiando reagenti come DCC e DMAP .
- L'anidride benzoica è formata dalla disidratazione dell'anidride acetica o del pentossido di fosforo.
- Derivati acidi altamente reattivi come gli alogenuri acilici sono facilmente ottenibili miscelando agenti come il cloruro di fosforo o il cloruro di tionile.
- Gli ortoesteri possono essere ottenuti dalla reazione di alcoli con benzonitrile in condizioni acide in assenza di acqua.
- La riduzione a benzaldeide e alcol benzilico avviene usando DIBAL-H , LiAlH 4 o sodio boroidruro.
Usi
Industria
Il 90% dell'acido benzoico in commercio è convertito in fenolo e caprolattame usato nella produzione di glicol-benzoati nell'industria della plastica. L'acido benzoico viene trasformato in fenolo mediante decarbossilazione ossidativa a 300-400 °C
Il fenolo poi può essere convertito in cicloesanolo, usato nella produzione del nylon. I plastificanti benzoati, come gli esteri di glicole, il dietilenglicole e il trietilenglicole, sono ottenuti per transesterificazione del metil benzoato con il diolo corrispondente. In alternativa, queste specie derivano dal trattamento del benzoilcloruro con diolo. I plastificanti sono usati in modo simile a quelli derivati dall'estere dell'acido tereftalico. L'acido benzoico è usato anche come attivatore e ritardante nella polimerizzazione della gomma.
Una ampia gamma dei suoi esteri è invece usata come solventi, additivi disinfettanti, agenti penetranti e come pesticidi.
Alimenti
L'acido benzoico (siglato come E 210) ed i suoi sali o esteri (siglati come E 211, E 212, E 213) sono usati come additivi alimentari. Il benzoato di sodio, il sale sodico dell'acido benzoico, è uno dei principali agenti anti-microbiotici usato nei cibi e nelle bevande poiché è 200 volte più solubile dell'acido benzoico.
La sua attività antimicrobica si esplica in seguito all'assobimento da parte delle cellule, dove modifica il pH, con conseguente inibizione degli enzimi ossoglutarato deidrogenasi e succinato deidrogenasi del ciclo di Krebs e di alcuni enzimi coinvolti nella fosforilazione ossidativa. L'efficacia dell'acido benzoico e del benzoato dipende quindi dal pH del cibo, per questo viene utilizzato principalmente in cibi e bevande acide come i succhi di frutta, bevande gassate o alcoliche e sottaceti. Agisce principalmente su lieviti e muffe e, solo in maniera secondaria, sui batteri.
Medicina
L'acido benzoico è un componente dell'unguento di Whitfield, che viene utilizzato per il trattamento di malattie della pelle fungine come tigna e piede d'atleta. L'acido benzoico è anche un ingrediente importante sia nella tintura di benzoino e nel balsamo di frate, usati come antisettici topici e decongestionanti delle vie aeree. Venne usato anche come espettorante, analgesico e antisettico. Indagini di laboratorio e lavori teorici molto recenti hanno evidenziato che l'acido benzoico e i suoi derivati sono promettenti per l'inibizione della SARS-CoV e COVID-19.
Biologia ed effetti sulla salute
L'acido benzoico è tossico a dosi eccessive (comunque inferiori al grammo, per individuo) la sua concentrazione è limitata al massimo allo 0,1%. Non viene accumulato nell'organismo ma escreto nelle urine sotto forma di acido ippurico. Si può trovare naturalmente in alcune piante, resine ed in alcuni animali. Quantità apprezzabili sono stati trovati nella maggior parte delle bacche (circa 0,05%). Frutti maturi delle specie di Vaccinium (ad esempio il mirtillo, V. vitis idaea, mirtillo nero, V. macrocarpon) contengono fino al 0,03-0,13% di acido benzoico.
L'acido benzoico si forma anche nelle mele dopo l'infezione con il fungo Nectria galligena. Tra gli animali, l'acido benzoico è stato identificato principalmente in specie onnivore o fitofage, ad esempio, in visceri e muscoli della pernice bianca (Lagopus muta), così come nelle secrezioni delle ghiandole di buoi muschiati di sesso maschile (Ovibos moschatus) o elefanti maschi asiatici (Elephas maximus). L'acido benzoico è anche uno dei composti chimici trovati nel castoreo, un composto raccolto dalle sacche dei castori nordamericani.
Il Cryptanaerobacter phenolicus è una specie batterica che produce benzoato dal fenolo attraverso il 4-idrossibenzoato.
Altri progetti
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su acido benzoico
Wikimedia Commons contiene immagini o altri file su acido benzoico
Collegamenti esterni
- (EN) Acido benzoico, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | Thesaurus BNCF 32771 · LCCN (EN) sh2003009190 · GND (DE) 4144531-4 · J9U (EN, HE) 987007566441405171 |
|---|