
Esametilfosforammide
| Esametilfosforammide | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| esametilfosforammide | |
| Nomi alternativi | |
| triammide esametilfosforica esametilfosfammide ossido di tri(dimetilammino)fosfina HMPA | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H18N3OP |
| Massa molecolare (u) | 179,20 |
| Aspetto | liquido incolore |
| Numero CAS | 680-31-9 |
| Numero EINECS | 211-653-8 |
| PubChem | 12679 |
| SMILES |
CN(C)P(=O)(N(C)C)N(C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,024 |
| Solubilità in acqua | completamente miscibile |
| Temperatura di fusione | 7,2 °C (280,35 K) |
| Temperatura di ebollizione | 233 °C (506,15 K) |
| Tensione di vapore (Pa) a 298,15 K | 9 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 2.650 (orale, ratto) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 105 °C (378,15 K) |
| Temperatura di autoignizione | 230 °C (503,15 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 350 - 340 |
| Consigli P | 201 - 308+313 |
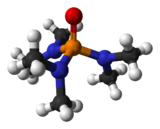
L'esametilfosforammide, spesso indicata con HMPA (abbreviazione dell'inglese Hexamethylphosphoramide), è l'ammide dell'acido fosforico con formula [(CH3)2N]3PO. A temperatura ambiente si presenta come un liquido incolore. Viene impiegata come solvente polare aprotico e come additivo nella sintesi organica.
Indice
Struttura e reattività
L'esametilfosforammide rappresenta l'ossido della fosfina terziaria altamente basica esametilfosfotriammide P(NMe2)3. Similmente ad altri ossidi di fosfina (per esempio l'ossido di trifenilfosfina), la molecola possiede un nucleo tetraedrico e un legame P-O altamente polarizzato, con una significativa carica negativa localizzata sull'atomo di ossigeno.
I composti che contengono un legame azoto-fosforo sono tipicamente degradati dall'acido cloridrico formando una ammina protonata e fosfato.
Applicazioni
L'HMPA è utilizzata come solvente per polimeri, gas e composti organometallici. Migliora la selettività delle reazioni di litiazione scindendo gli oligomeri formati dalle basi di litio come il butillitio. Dato che l'esametilfosforammide solvata selettivamente i cationi, questo solvente è in grado di accelerare alcune reazioni SN2 difficoltose. L'atomo basico di ossigeno nell'HMPA coordina fortemente il catione Li+. Un complesso del perossido di molibdeno con l'esametilfosforammide viene utilizzato come ossidante nella sintesi organica.
Reagenti alternativi
Il dimetilsolfossido può essere spesso utilizzato come solvente in sostituzione dell'HMPA. Sono entrambi forti accettori di legame idrogeno, e i loro atomi di ossigeno legano i cationi metallici. Altre alternative all'HMPA includono le tetraalchiluree e le alchiluree cicliche come DMPU.
Tossicità
L'esametilfosforammide è tossica ed è stata dimostrata in grado di indurre il cancro nasale nei ratti. L'HMPA può essere degradata a composti meno tossici per azione dell'acido cloridrico.
Altri progetti
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su Esametilfosforammide
Wikimedia Commons contiene immagini o altri file su Esametilfosforammide
Collegamenti esterni
| Controllo di autorità | GND (DE) 4159805-2 |
|---|