
Tamoxifene
| Tamoxifene | |
|---|---|
 | |
 | |
| Nome IUPAC | |
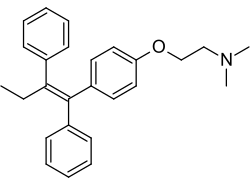
| (Z)-2-[4-(1,2-Diphenyl-1-butenyl)phenoxy]-N,N-dimethylethanamine | |
| Nomi alternativi | |
| tamossifene | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C26H29NO |
| Massa molecolare (u) | 371,51 |
| Numero CAS | 10540-29-1 |
| Numero EINECS | 234-118-0 |
| Codice ATC | L02BA01 |
| PubChem | 5376 |
| DrugBank | DB00675 |
| SMILES |
CCC(=C(C1=CC=CC=C1)C2=CC=C(C=C2)OCCN(C)C)C3=CC=CC=C3 |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 96-98 °C |
| Dati farmacocinetici | |
| Emivita | 5–7 giorni |
| Escrezione | fecale |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 350 - 360 - 362 |
| Consigli P | 201 - 263 - 308+313 |
Il tamoxifene o tamossifene è un farmaco antitumorale assunto per via orale e appartenente alla famiglia dei modulatori selettivi del recettore degli estrogeni (SERM).
Indice
Storia
Lo sviluppo del tamoxifene ha origine da un'area di ricerca che aveva un ampio interesse negli anni sessanta del Novecento, ovvero quella che riguardava i farmaci contraccettivi; si era visto infatti inizialmente che gli antiestrogeni avevano attività come contraccettivi post-coitali negli animali da esperimento, ma nell'uomo poi si vide che inducevano l'ovulazione in donne subfertili. L'interesse verso gli antiestrogeni in questo ambito svanì quindi con questa evidenza clinica, ma il fallimento di questa applicazione diventò un'opportunità per sviluppare dei farmaci contro il tumore alla mammella.
La dipendenza dagli ormoni nella crescita di alcuni tumori al seno si conosceva fin dal 1896, quando il dottor George Beatson riportò che una donna con un cancro al seno metastatico in stadio avanzato rispose sensibilmente alla rimozione delle sue ovaie, che sono gli organi preposti alla sintesi degli ormoni femminili. Altri studi rilevarono che solo una donna su tre rispondeva all'intervento di rimozione e non c'era un modo di sapere quali pazienti avrebbero risposto. Nel 1971 il dottor Elwood Jensen scoprì che esisteva un recettore per gli estrogeni (ER) che mediava l'azione di questi ormoni in particolari tessuti e applicò questo concetto con successo tanto da elaborare un test predittivo per il trattamento del cancro al seno: tramite una biopsia del tumore, il test mira a verificare o meno la presenza dei recettori ER e quindi la risposta della paziente alla terapia sia di rimozione delle ovaie sia alla terapia farmacologica con molecole estrogene sintetiche.


Il primo antiestrogeno non steroideo scoperto fu il MER25 (etamoxitrifetolo), che pur avendo una struttura simile agli estrogeni sintetici, quella del trifeniletanolo, aveva attività antagonista verso il recettore ER. Tuttavia questo farmaco destava preoccupazioni per la sua possibile tossicità se usato in terapie a lungo termine come quella richiesta nel tumore al seno. Questo perché era un derivato strutturale del farmaco ipocolesterolemizzante triparanolo, che era stato ritirato dal commercio: i suoi effetti sui livelli di colesterolo infatti sembravano far aumentare i livelli di desmosterolo e questo si pensava provocasse una maggiore incidenza di cataratta in donne giovani. Di conseguenza, solo farmaci che non modificassero i livelli circolanti di desmosterolo sarebbero stati accettati per una terapia a lungo termine.
Nel 1962, una chimica di nome Dora Richardson sintetizzò il composto ICI46,474, che poi divenne il tamoxifene; lei faceva parte di un team di endocrinologi riproduttivi della Divisione Farmaceutica presso le Imperial Clinical Industries (ora AstraZeneca), a capo della quale c'era il biologo Arthur Walpole. Nel 1967 si scoprì che l'isomero trans di ICI46,474 aveva una parziale attività agonista/antagonista nel ratto mentre aveva una piena attività agonista nel topo, inoltre abbassava i livelli di colesterolo circolante senza alzare i livelli di desmosterolo. Uno studio successivo del 1969 dimostrò che il tamoxifene ad alte dosi induceva l'ovulazione, mentre a basse dosi tendeva ad avere un'azione anti-estrogenica.
C'era però una certa riluttanza nel continuare lo sviluppo di tale farmaco essendo un trattamento palliativo a breve termine per il cancro al seno in fase avanzata. Diversi fattori vennero considerati nella decisione di non proseguire lo sviluppo: la classe di composti non aveva il brevetto negli USA (fu posto nel 1985), inoltre non si riteneva significativo il mercato per un farmaco palliativo che sarebbe stato efficace per un anno in una paziente su tre, non c'erano poi infrastrutture per supportare un programma contro il tumore al seno, e soprattutto era opinione comune che un'altra terapia endocrina non avrebbe aggiunto niente alla lista di terapie contro il cancro al seno.
Nel 1971 uno studio sull'ICI46,474 condotto dal dottor Lars Terenius del dipartimento di farmacologia a Lund, in Svezia, per il trattamento del cancro al seno in pazienti in post-menopausa, mostrò una certa efficacia accompagnata da un profilo migliore per quanto riguardava gli effetti collaterali rispetto agli altri estrogeni o androgeni.
Nell'ottobre del 1973, ICI46,474 uscì nel Regno Unito come farmaco per l'infertilità e come trattamento palliativo del cancro al seno. Nonostante questo, fu sviluppata una strategia per un'appropriata applicazione clinica del farmaco in modo da dirigerlo nelle masse tumorali che avrebbero risposto, cioè quelle la cui crescita è estrogeno-dipendente.
La strategia iniziale per la valutazione del tamoxifene fu l'uso per un anno come terapia adiuvante dopo intervento chirurgico; si temeva infatti che un trattamento più lungo avrebbe causato resistenza al farmaco. Tuttavia, la seguente valutazione di due o cinque anni di terapia adiuvante di pazienti in pre-menopausa con tumore ER positivo mostrò un aumento della sopravvivenza, mentre un anno di terapia non si dimostrò efficace. Con l'aumento della durata della terapia a dieci anni invece, risultò un aumento di ricomparse di tumori e di effetti collaterali (cancro all'endometrio, coaguli di sangue), effetti assenti nella terapia di cinque anni. Questa resistenza al tamoxifene sembrava dovuta soprattutto al fatto che le cellule tumorali crescevano stimolate dal farmaco a livello del seno e dell'endometrio.
La terapia di cinque anni con tamoxifene divenne quindi il trattamento di prima scelta negli anni 1990, grazie anche al vantaggio che dopo la sospensione della terapia l'effetto durava per almeno altri dieci anni; questo probabilmente perché il farmaco modifica la struttura delle cellule tumorali in modo che, dopo la sospensione, le basse concentrazioni di estrogeni rimaste, uccidano le cellule tumorali.
C'erano inoltre numerose evidenze scientifiche che portavano a pensare che il farmaco potesse essere utile per prevenire il tumore al seno: nel 1992 partì negli Stati Uniti uno studio clinico randomizzato su 13 800 volontarie per testare il tamoxifene come agente preventivo per ridurre l'incidenza di cancro al seno in donne ad alto rischio. Ne risultò una diminuzione del 50% in pazienti trattate con tamoxifene rispetto alle pazienti trattate con placebo. Gli attesi effetti collaterali (aumento d'incidenza di trombi e tumore all'endometrio) furono notati solo in donne in post-menopausa. Nel 1998 il tamoxifene fu approvato dall'FDA per la riduzione del rischio di cancro al seno in donne in pre- e post- menopausa.
Farmacodinamica
Il tamoxifene presenta un meccanismo d'azione complesso e non ancora chiaramente definito. Il principale bersaglio di questo farmaco è il recettore per gli estrogeni (ER), il quale è un recettore nucleare presente in due diverse isoforme: ERα ed ERβ. Il tamoxifene agisce legandosi al recettore in competizione con il substrato endogeno, l'estradiolo, con una diversa modalità nei confronti delle due isoforme α e β: è un parziale agonista verso ERα, mentre è un totale antagonista nei confronti di ERβ. L'azione del tamoxifene può essere quindi sia pro-estrogena sia anti-estrogena in relazione al tessuto in cui agisce: l'effetto finale dipende dal rapporto di recettori ERα/ERβ presenti e dall'insieme di co-attivatori e co-repressori espressi in una determinata cellula con cui il recettore ER può interagire.
Tuttavia, anche nello stesso tessuto, il tamoxifene può avere effetti opposti. Ad esempio, nel tessuto mammario induce i recettori del progesterone (effetto agonista), mentre inibisce la crescita del cancro al seno (effetto antagonista) nello stesso seno.
Questa azione antagonista risulta essere essenziale nel trattamento di tumori al seno estrogeno-dipendenti, in cui lo sviluppo e la crescita della massa tumorale è favorita dalla presenza di ormoni estrogeni. Dal punto di vista molecolare, il farmaco interagisce con il recettore legandosi a livello del Ligand Binding Domain, sito a cui dovrebbe legarsi l'estrogeno endogeno.
A seguito di questo legame, il complesso tamoxifene-recettore recluta delle molecole chiamate co-repressori e lega il DNA in specifiche regioni chiamate ERE (Estrogen response elements). In questo modo il tamoxifene modula l'espressione genica riducendo l'attività degli estrogeni. In modo particolare induce un arresto della crescita cellulare, bloccando le cellule tumorali allo stato G0/G1 del ciclo cellulare.
Un altro meccanismo suggerito per questa azione antiproliferativa è l'induzione da parte del tamoxifene della sintesi da parte delle cellule tumorali del fattore di crescita trasformante citochina-β (TGF-β), una citochina che agisce come una molecola regolatrice negativa autocrina, cioè induce la morte delle cellule tumorali stesse.
Tuttavia, è stato dimostrato che il tamoxifene può indurre la sintesi del TGF-β anche nelle cellule che non esprimono il recettore degli estrogeni.
Farmacocinetica
Assorbimento
Il tamoxifene è assorbito rapidamente nel tratto gastrointestinale. La sua biodisponibilità, ossia la frazione di farmaco che raggiunge il circolo sistemico immodificato, è elevata (approssimativamente del 100%) e indipendente dalla dose in quanto subisce uno scarso effetto di primo passaggio. A seguito della somministrazione di una dose di 40 mg di tamoxifene, la concentrazione plasmatica massima (Cmax) raggiunta è di circa 65 µg/L e si registra dopo circa 3-4 ore dalla somministrazione.
Distribuzione
Il tamoxifene ha elevata affinità di legame per le proteine plasmatiche, specie per l'albumina (maggiore del 95%). La sua distribuzione è stata studiata in tessuti animali mediante l'utilizzo del [C14] tamoxifene: elevata radioattività è stata registrata nel tessuto mammario, nell'utero, nel fegato, nei reni, polmoni e pancreas. Nell'uomo il volume di distribuzione è di circa 60 L/kg.
Metabolismo
Il tamoxifene subisce metabolismo di fase I nel fegato per opera della famiglia dei citocromi P450. I metaboliti che si formano derivano dalla sua idrossilazione, demetilazione e coniugazione e come tali essi agiscono similmente al farmaco immodificato contribuendo all'effetto terapeutico. Le isoforme dei citocromi che intervengono nel metabolismo del tamoxifene sono CYP3A4, CYP2C19 e CYP2D6. I metaboliti che si formano sono N-demetiltamoxifene, che si forma per N-demetilazione del tamoxifene per opera del CYP3A4, e il 4-idrossitamoxifene o afimoxifene, che si forma per idrossilazione in posizione 4 del tamoxifene per opera del CYP2D6. L'N-demetiltamoxifene è un metabolita attivo con minor affinità per il recettore degli estrogeni (ER) rispetto al tamoxifene; esso può essere ulteriormente metabolizzato per idrossilazione per opera del CYP2D6 formando un altro metabolita attivo detto endoxifene (N-demetil-4-idrossitamoxifene). Afimoxifene ed endoxifene sono metaboliti attivi con un'affinità da 30 a 100 volte maggiore per il recettore degli estrogeni (ER) rispetto al tamoxifene stesso. Il tamoxifene ha solamente il 6% e il 7% dell'affinità dell'estradiolo rispettivamente per i recettori ERα e ERβ mentre l'endoxifene ha il 178% e il 338% dell'affinità dell'estradiolo per ERα ed ERβ.
La concentrazione sierica del tamoxifene allo stato stazionario è raggiunta dopo circa 3-4 settimane per dosaggi pari a 20 mg/die o 40 mg/die. Le concentrazioni medie allo steady-state variano tra 164-494 µg/L, per somministrazione di 20 mg/die e 186-214 µg/L, per dosaggi pari a 40 mg/die. L'area sottesa alla curva (AUC), per somministrazione di 10 mg di tamoxifene due volte al giorno per 21 giorni, è di 1 597 µg*h/L.
Escrezione
Il tamoxifene è escreto con la bile ed eliminato per via fecale mentre solo una piccola parte per via renale. L'emivita di eliminazione (τβ) del tamoxifene immodificato è di 5-7 giorni e dipende dalla circolazione enteroepatica, dal legame del farmaco con le proteine plasmatiche e dall'autoinibizione del metabolismo. L'emivita di eliminazione invece dell'N-demetiltamoxifene è di circa 14 giorni.
Usi
Carcinoma mammario
Il tamoxifene è utilizzato nel trattamento del carcinoma mammario precoce e avanzato positivo al recettore per gli estrogeni nelle donne sia in pre-menopausa sia in post-menopausa. È inoltre utilizzato per la prevenzione del carcinoma al seno nelle donne predisposte alla malattia. Il tamoxifene è stato inoltre approvato per il trattamento del cancro controlaterale ed è utilizzato anche nel trattamento ormonale del cancro al seno maschile.
Infertilità
Nella donna i modulatori selettivi del recettore estrogenico non steroidei (SERM), come il tamoxifene e il clomifene, sono comunemente usati per indurre l'ovulazione. Il clomifene induce l'ovulazione agendo a livello ipotalamico sul recettore per gli estrogeni con effetto antagonista mentre il tamoxifene, con lo stesso effetto, agisce come un agonista sui recettori degli estrogeni della mucosa vaginale e dell'endometrio.
Nell'uomo iI tamoxifene agisce con effetto antiestrogenico a livello ipotalamico occupando il recettore degli estrogeni. Quest'azione induce un aumento della secrezione di GnRH a livello ipotalamico che porta a un successivo aumento del rilascio delle gonadotropine quali l'ormone luteinizzante (LH) e follicolo-stimolante (FSH) da parte dell'ipofisi anteriore che stimolano la secrezione di testosterone. L'aumento di testosterone si traduce in un aumento della densità del liquido spermatico e del numero degli spermatozoi vivi. Il tamoxifene sembra non avere effetto invece sulla motilità e la morfologia degli spermatozoi. Un significativo aumento di questi parametri è stato verificato però solo in uomini affetti da oligozoospermia e oligospermia ma non in uomini normozoospermici.
Ginecomastia
Il tamoxifene, agendo come modulatore dei recettori per gli estrogeni, riduce i sintomi della ginecomastia primaria, in alcuni casi promuove anche la risoluzione della patologia e viene inoltre utilizzato come misura preventiva in piccole dosi o alle prime manifestazioni di qualsiasi sintomo come dolore o sensibilità al capezzolo. La ginecomastia è una condizione che porta a un accrescimento atipico del tessuto mammario maschile dovuto a una relativa iperattività degli estrogeni. Può essere primaria o secondaria e in quest'ultimo caso può essere dovuta all'assunzione di particolari farmaci, per patologie epatiche, insufficienza renale o per disordini genetici o maligni. La ginecomastia è solitamente asintomatica ma può anche manifestarsi con un gonfiore vicino all'areola.
Effetti collaterali
Effetti collaterali ginecologici
Questi effetti collaterali dipendono, oltre che dal tessuto specifico, dalla concentrazione di estradiolo presente e quindi da un eventuale stato di menopausa della paziente.
A livello dell'epitelio vaginale sono state registrate delle variazioni in pazienti in post-menopausa in seguito al trattamento prolungato con tamoxifene: sono state evidenziate molte candidiasi vulvovaginali, di solito rare in condizioni di post-menopausa perché queste infezioni richiedono un tessuto molto ricco di glicogeno per proliferare. Per spiegare questi sintomi, attraverso degli studi è stato dimostrato che il tamoxifene ha un'azione estrogeno-simile a livello dell'epitelio vaginale di queste pazienti. In donne più giovani non ancora entrate nella menopausa (che quindi presentano alte concentrazioni di estrogeni a livello vaginale) il tamoxifene ha invece un effetto opposto, ovvero azione estrogeno-antagonista. A questo effetto possono conseguire secchezza vaginale e problemi nei rapporti sessuali.
Il tamoxifene si è dimostrato capace d'indurre un aumento del rischio dello sviluppo del cancro all'endometrio. L'effetto del farmaco sull'endometrio dipende dalla concentrazione dei recettori ER presenti e sembra agire come un estrogeno-agonista solo in pazienti in post-menopausa. Questo avviene perché nell'endometrio l'aumento dei livelli di estrogeni indotto dal tamoxifene provoca la stimolazione della crescita epiteliale e un aumento dell'espressione dei recettori dei progestinici. Per quanto riguarda le pazienti non ancora entrate in menopausa non sono state registrate differenze rispetto a donne non trattate, il che suggerisce un effetto estrogeno-antagonista del tamoxifene in un ambiente ricco di estrogeni. Quindi il tamoxifene in questa classe di pazienti non sembra aumentare il rischio di sviluppare il cancro all'endometrio, ma provoca alcuni effetti meno severi: ad esempio il ciclo mestruale diventa irregolare, oligomenorreico o amenorreico.
Per quanto riguarda l'endometriosi, questa si verifica quasi esclusivamente nelle donne in età riproduttiva. Tuttavia sono stati registrati dei casi anche in pazienti in postmenopausa che assumono il tamoxifene. In questa classe di soggetti, i recettori degli estrogeni e i recettori del progesterone sono stati descritti in concentrazioni simili a quelle di donne in pre-menopausa non trattate con tamoxifene. Poiché l'endometriosi è una malattia estrogeno-dipendente, il meccanismo d'azione probabilmente è dato dalla stimolazione del tessuto endometriale ectopico anche nelle donne in post-menopausa, in virtù dell'attività estrogeno-agonista del tamoxifene.
A livello delle ovaie, Klopper e Hall nel 1971 descrissero per primi gli effetti del tamoxifene: esso è in grado di indurre l'ovulazione in donne non fertili che non sono in grado di ovulare, portando a un aumento delle concentrazioni sieriche di estrogeni e progesterone. In donne in pre-menopausa il tamoxifene induce la produzione di estrogeni nell'ovaio, mentre i livelli di FSH e LH non aumentano o lo fanno solo leggermente. Sempre a livello ovarico il tamoxifene può portare alla formazione di cisti.
Per quando riguarda la sfera psicosessuale, il tamoxifene provoca in molte pazienti una riduzione della libido sessuale. Questo fenomeno può essere dovuto a sintomi dovuti principalmente all'attività anti-estrogena del farmaco, che possono essere più o meno marcati in base al soggetto: vampate di calore, secchezza vaginale, emicranie, ecc. Gli effetti più marcati sulla sessualità si riscontrano nella fascia di pazienti a cui il trattamento con tamoxifene induce una condizione di menopausa prematura, mentre nelle donne già in menopausa la riduzione dell'attività sessuale risulta essere meno significativa.
Effetti collaterali cardiovascolari
Il tamoxifene ha dimostrato avere un effetto benefico sul profilo lipidico sierico: in pazienti in post-menopausa è stata registrata una diminuzione sia del colesterolo sia delle LDL, probabilmente dovuto alla parziale attività agonista a livello dei recettori ER. Però il tamoxifene sembra non avere effetti positivi sui trigliceridi: i livelli sierici in seguito al trattamento tendono ad aumentare e possono causare ipertrigliceridemia.
I diversi effetti sulle concentrazioni di colesterolo e dei trigliceridi nel sangue suggeriscono che il farmaco non ha un effetto cardioprotettivo, cioè non porta a un beneficio clinicamente rilevante rispetto allo sviluppo o alla progressione di patologie cardiovascolari. Infatti il tamoxifene sembra provocare un aumento dell'incidenza di infarto, embolia polmonare ed eventi di tromboembolismo venoso.
Effetti collaterali ossei
Il trattamento con tamoxifene nelle donne in post-menopausa induce una riduzione della perdita di densità ossea, il che suggerisce un'azione estrogeno-agonista del farmaco a livello del tessuto osseo. In modo particolare il tamoxifene aumenta l'espressione di FasL (ligando del recettore Fas) a livello degli osteoblasti, provocando l'apoptosi dei pro-osteoclasti e quindi riducendo i processi di demineralizzazione dell'osso.
Questa attività estrogeno-agonista del tamoxifene a livello del tessuto osseo si verifica però solo in condizioni in cui vi sia un basso livello di estrogeni endogeni nell'organismo. Infatti nelle donne in pre-menopausa, che presentano alti livelli di estrogeni, il farmaco ha azione estrogeno-antagonista e provoca perdita di densità ossea. Induce invece un certo grado di protezione dalla demineralizzazione ossea nelle donne in cui si è sviluppata una menopausa precoce indotta dalla chemioterapia.
Effetti collaterali centrali
Il trattamento con tamoxifene nelle donne in post-menopausa può portare a una condizione di ipometabolismo nei lobi laterali (frontali e dorsali) del cervello a causa di una minor capacità di utilizzare glucosio. Sono state registrate anche significative riduzioni della memoria semantica.
Effetti collaterali alla vista
In donne trattate con alte dosi di tamoxifene sono stati registrati casi di retinopatie, ovvero disturbi a livello della retina, mentre in donne trattate con dosi standard questi effetti collaterali sono molto più ridotti. Inoltre il trattamento con tamoxifene è associato a un lieve aumento dell'incidenza di cataratta.
Interazioni
La contemporanea assunzione di anticoagulanti orali come il warfarin può essere pericolosa perché il tamoxifene ne aumenterebbe significativamente l'attività anticoagulante causando emorragie; il meccanismo di interazione è sconosciuto ma si pensa che sia coinvolta la competizione per il legame alle proteine plasmatiche, poiché il tamoxifene è molto legato alle proteine. In questi casi si monitorano gli indici di coagulazione e si diminuiscono le dosi di warfarin.
La rifampicina, un farmaco antibatterico usato nel trattamento della tubercolosi, induce diverse isoforme di citocromi tra cui il CYP3A4, coinvolto nel metabolismo del tamoxifene, che assunto con la rifampicina viene eliminato più velocemente e quindi ha una minore concentrazione plasmatica.
L'associazione con inibitori dell'aromatasi, altri farmaci per trattare il tumore al seno, non ha mostrato miglioramenti nell'efficacia ma è stato visto che la combinazione dei due farmaci altera la farmacocinetica del tamoxifene: quest'ultimo vedrebbe infatti ridotte le sue concentrazioni plasmatiche. È dunque da tenere presente questa interazione quando si valuta l'efficacia della terapia di combinazione.
Il letrozolo, che fa parte degli inibitori dell'aromatasi, non altera invece il metabolismo del tamoxifene, ma al contrario è il tamoxifene che provoca una diminuzione delle concentrazioni plasmatiche di letrozolo.
Possibili interazioni si possono riscontrare con inibitori del citocromo CYP2D6, con riduzione del 65% – 75% dei livelli plasmatici di un metabolita attivo del tamoxifene, il 4-idrossi-N-desmetiltamoxifene (endoxifene). In alcuni studi, è stata riportata una ridotta efficacia del tamoxifene quando somministrato in concomitanza con alcuni antidepressivi inibitori selettivi del reuptake della serotonina SSRI (ad es. paroxetina, fluoxetina); è quindi preferibile evitare l'associazione di questi farmaci.
Gravidanza e allattamento
L'assunzione di tamoxifene è controindicata in gravidanza. Infatti, nonostante non sia stata stabilita nessuna relazione causale con il farmaco, sono stati segnalati alcuni casi di aborti spontanei, anomalie congenite e morti fetali in pazienti che avevano assunto il principio attivo.
Negli studi di tossicità sul ciclo riproduttivo nel ratto, coniglio e scimmia, il tamoxifene non ha mostrato potenziale teratogeno. Nei modelli sperimentali di sviluppo del tratto riproduttivo fetale del roditore, tamoxifene è stato associato a modificazioni simili a quelle causate da estradiolo, etinilestradiolo, clomifene e dietilstilbestrolo (DES), come l'adenosi vaginale.
I potenziali rischi per il feto possono esserci anche se s'instaura una gravidanza nei due mesi successivi all'interruzione della terapia.
L'allattamento non è consigliato durante il trattamento con tamoxifene, in quanto non è noto se il farmaco sia escreto nel latte materno.
Pazienti speciali
In pazienti con insufficienza renale è stato visto che c'è un così ridotto effetto sulla farmacocinetica del tamoxifene (e su tutti i SERM, modulatori selettivi del recettore degli estrogeni) che può essere trascurato. Il tamoxifene infatti viene eliminato prevalentemente nella bile e nelle feci, mentre solo una piccola percentuale è eliminata con le urine.
Poiché la via principale di eliminazione dei SERM è quella epatica, se una paziente ha qualche patologia del fegato questa può influenzare la farmacocinetica del tamoxifene. Su questo farmaco però non sono stati fatti molti studi al riguardo: uno solo ha mostrato che in un paziente con un'ostruzione epatica, le concentrazioni ematiche di tamoxifene aumentavano. Un altro studio ha invece mostrato che l'assunzione di tamoxifene può aggravare le condizioni di un fegato già steatosico o rallentarne la guarigione.
La farmacocinetica del tamoxifene è influenzata anche dall'età, infatti uno studio rivela che maggiore è l'età di una donna e maggiori sono le concentrazioni ematiche di farmaco: su donne con meno di 40 anni si sono viste concentrazioni di circa 249 nmol/L, mentre su donne con più di 80 anni si sono viste concentrazioni di 656 nmol/L.
Tamoxifene come farmaco orfano
Il 22 maggio 2017 la Commissione europea ha concesso all'azienda GB Pharma di Pavia la designazione del tamoxifene citrato come farmaco orfano per la fibrosi cistica. Il farmaco aumenta infatti l'attività di una proteina chiamata "canale dei cloruri calcio-dipendente" (CaCC), coinvolta nella regolazione della produzione di muco e di succhi gastrici. Questo aiuterebbe a diminuire le eccessive secrezioni che si riscontrano nella fibrosi cistica, migliorando i sintomi di questa malattia e le funzioni polmonari.
Il 12 ottobre 2017 la Commissione europea ha concesso all'azienda Duchenne UK la designazione del tamoxifene citrato come farmaco orfano per la distrofia muscolare di Duchenne. Il farmaco infatti, agendo sui recettori per gli estrogeni anche nei muscoli, ne aumenterebbe la forza e la riparazione; inoltre proteggerebbe le cellule muscolari da diversi tipi di danni che si riscontrano nella distrofia di Duchenne. Questi effetti sono stati osservati in modelli sperimentali, ma al momento della designazione come farmaco orfano non era stato effettuato nessuno studio clinico.
Bibliografia
- Thomas L. Lemke, David A. Williams, Victoria F. Rocke, S. William Zito, FOYE'S, Principi di chimica farmaceutica, Sesta edizione italiana, Ed. Piccin
Voci correlate
Altri progetti
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su tamoxifene
Wikimedia Commons contiene immagini o altri file su tamoxifene