
Tigeciclina
| Tigeciclina | |
|---|---|
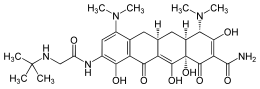 | |
| Nome IUPAC | |
| N-[(5aR,6aS,7S,9Z,10aS)-9-[ammino(idrossi)metilidene]-4,7-bis(dimetilammino)-1,10a,12-triidrossi-8,10,11-triosso-5,5a,6,6a,7,8,9,10,10a,11-decaidrotetracen-2-yl]-2-(tert-butilammino)acetammide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C29H39N5O8 |
| Massa molecolare (u) | 585,65 g/mol |
| Numero CAS | 220620-09-7 |
| Numero EINECS | 685-736-6 |
| Codice ATC | J01AA12 |
| PubChem | 5282044 CID 5282044 |
| DrugBank | DB00560 |
| SMILES |
CC(C)(C)NCC(=O)NC1=CC(=C2C(=C1O)C(=O)C3=C(C4(C(CC3C2)C(C(=C(C4=O)C(=O)N)O)N(C)C)O)O)N(C)C |
| Dati farmacologici | |
| Categoria farmacoterapeutica | Glicilcicline |
| Teratogenicità | classe D (valutazione ADEC) |
| Modalità di somministrazione |
endovena |
| Dati farmacocinetici | |
| Biodisponibilità | NA |
| Metabolismo | Non metabolizzato |
| Emivita | 42.4 ore |
| Escrezione | biliare, renale |
| Indicazioni di sicurezza | |
La tigeciclina è un antibiotico glicilciclinico sviluppato da Francis Tally e prodotto dalla casa farmaceutica Wyeth con il nome di Tygacil. Ha ricevuto l'approvazione della Food and Drug Administration (FDA) il 17 giugno 2005. È stato sviluppato in seguito agli episodi di resistenza agli antibiotici di alcuni batteri che sviluppano pompe di efflusso, quali Staphylococcus aureus e Acinetobacter baumannii.
Indice
Meccanismo d'azione
La tigeciclina è un batteriostatico che interferisce con la sintesi delle proteine batteriche legandosi in modo reversibile alla subunità ribosomiale 30S, bloccando l'entrata dell'ammino-acil tRNA nel sito A del ribosoma.
Dosaggi
La tigeciclina è somministrata per infusione venosa lenta (da 30 a 60 minuti). La dose iniziale è di 100 mg, seguita da dosi di 50 mg ogni dodici ore. I pazienti con funzioni vitali compromesse possono necessitare di dosaggi più bassi. Ai pazienti con disfunzioni epatiche è solitamente prescritta una dose di mantenimento di 25 mg ogni dodici ore in luogo degli usuali 50 mg, l'alterazione renale non è invece motivo di variazione. Non sono previste dosi pediatriche, non essendo consigliata per i bambini, e non esistono forme di somministrazione orale.
Usi clinici
La tigeciclina è attiva contro i batteri Gram positivi e Gram negativi, compresi batteri resistenti alle tetracicline, e contro alcuni anaerobi. È attiva anche contro Staphylococcus aureus resistente alla meticillina e contro gli enterococchi resistenti alla vancomicina, anche se molti ceppi di Proteus e di Pseudomonas aeruginosa ne sono resistenti. È impiegata inoltre nelle terapie sperimentali contro il C. difficile. L'uso della tigeciclina deve essere riservato al trattamento delle infezioni complicate della cute e dei tessuti molli e delle infezioni complicate dell'addome causate da microrganismi resistenti a più antibiotici.
Effetti collaterali
La tigeciclina ha effetti collaterali simili a quelli delle tetracicline.
I più comuni tra questi sono diarrea, nausea e vomito. Nausea e vomito si protraggono solitamente per i primi due giorni della terapia.
Altri effetti indesiderati includono dolore nel sito di iniezione, gonfiore e irritazione.
È vietato l'utilizzo su bambini e donne in stato di gravidanza a causa dei danni provocati su ossa e denti.
Come per tutti gli antibiotici è possibile un aumento del numero di batteri resistenti.
Bibliografia
- Opinion of the Committee for Medicinal Products for Human Use on the Granting of a Marketing Authorisation for Tygacil(TM) (tigecycline) - Annex I: Summary of Product Characteristics. London, UK: European Medicines Agency, February 23, 2006.
- Goosens H, Ferech M, Stichele RV, et al, for the ESAC Project Group. Outpatient antibiotic use in Europe and association with resistance; a cross-national database study. Lancet. 2005; 365: 579-587.
- Shlaes DM, Gerding DN, John JF Jr, et al. Society for Healthcare Epidemiology of America and Infectious Diseases Society of America Joint Committee on the Prevention of Antimicrobial Resistance: Guidelines for the Prevention of Antimicrobial Resistance in Hospitals. Clin Infec Dis. 1997; 25: 584-599.
- Cosgrove SE, Carmeli Y. The impact of antimicrobial resistance on health and economic outcomes. Clin Infect Dis. 2003; 36: 1433-1437.
- Levy SB. Active efflux, a common mechanism for biocide and antibiotic resistance. J App Microbiol. 2002; 92: 65S-71S.
- Poole K. Mechanisms of bacterial biocide and antibiotic resistance. J App Microbiol. 2002; 92: 55S-64S.
- Paolo Romanelli, Kerdel Franciso A, Trent Jennifer T, Manuale di terapia dermatologica, Milano, McGraw-Hill, 2006, ISBN 88-386-3913-2.
Altri progetti
Altri progetti
-
 Wikimedia Commons contiene immagini o altri file su Tigeciclina
Wikimedia Commons contiene immagini o altri file su Tigeciclina
Collegamenti esterni
- (EN) Tygacil ( tigecycline iv ): Antibiotic for Skin Infections, su tygacil.com. URL consultato il 3 febbraio 2012 (archiviato dall'url originale il 6 luglio 2008).
- informazionisuifarmaci.it, http://www.informazionisuifarmaci.it/database/fcr/sids.nsf/stampa/482D8EC38C560D70C12573AA002E4FE6?OpenDocument Titolo mancante per url
url(aiuto).